농림축산검역본부(본부장 김정희, 이하 검역본부)는 동물용의약품 산업 발전 대책 마련 전담 조직(TF) 제3차 제도개선·연구개발(R&D) 분과 회의를 지난 4일 개최했다고 밝혔습니다.

이번 회의에서는 동물약품 업계 관계자와 수의과대학, 동물약품협회, 수의사회 등 관련기관 전문가 20여 명이 참석했습니다. 동물용의약품 제조·품질관리 기준(GMP) 선진화, 신약개발 및 산업 역량제고를 위한 연구개발(R&D) 확대, 수출 활성화를 위한 동물약품 인·허가 제도개선 과제 추진 상황 등을 논의했습니다.
지난 2월 농림축산식품부에서 동물용의약품 산업의 수출 경쟁력을 확대하고 지속 가능한 산업 조성을 위해 ‘동물용의약산업 발전 대책 수립 전담 조직(TF)’를 구성(팀장: 방역정책국장, 총괄·제도개선·연구개발(R&D) 3개 분과)하여 운영하고 있으며, 검역본부는 제도개선과·연구개발(R&D) 분과 운영을 담당하고 있습니다.
이에 따라, 검역본부는 각 분과별로 전문가 조직을 구성해 2월 16일 자체 첫 회의(kick-off)를 시작으로, 팀별 회의(3회) 및 현장 간담회를 통해 업계와 소통하며 동물용의약품 제조·품질관리 기준(GMP) 선진화 방안, 관련 제도 정비, 연구개발(R&D) 확대 등 체계적 지원 방안 마련을 위해 추진과제 발굴 및 세부계획을 수립하고 있습니다.
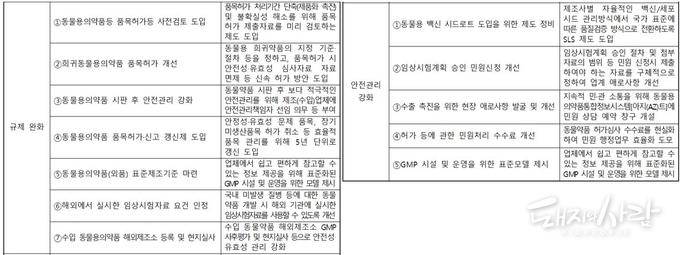
이날 회의에서 제도개선 분과는 국내 동물용의약품 제조·품질관리 기준(GMP) 기준 선진화 방안 마련을 위한 전문가 용역 추진상황과 수출 경쟁력 제고를 위한 동물용의약품 제조·품질관리 기준(GMP) 관련 국제협의체(PIC/S) 가입 추진 조건·절차에 대한 정보를 공유하고, 동물용의약품 신속 인허가 등을 위한 행정서비스 개선과 동물약품 안전관리 강화와 관련된 제도개선 세부과제(12개) 추진내용에 대해서도 전문가와 함께 점검했습니다.
또한, 연구개발(R&D) 지원 확대를 위한 민간협력 강화, 정부기관 특수연구시설 개방, 전문인력 양성, 동물질병자원 바이오뱅크 구축 방안 등 과제 검토와 함께 동물용 신약의 허가 속도 개선 및 불확실성 해소를 위해 연구개발 사전 상담부터 일관된 서비스를 제공하는 신약 기술검토팀 운영에 대한 설명이 있었습니다.
이날 회의를 주재한 이명헌 동물질병관리부장은 “이번 동물용의약품 산업 발전 대책에는 업계가 충분히 공감하고 수용할 수 있는 실효적인 개선 대책 마련이 무엇보다 중요하며, 이를 위해 검역본부는 업계와 전문가의 다양한 의견을 모을 수 있도록 지속적으로 소통하겠다”라고 말했습니다.
한편 농림축산식품부는 올해 동물용 의약품․의료기기 관련 예산을 대폭 확대('23. 105억원 → '24. 137) 하였습니다. 경쟁력 있는 제품 생산 및 수출 지원을 위한 원료구입 자금 지원을 확대하고, 해외 전시회 한국관 운영 등 판로·마케팅 지원 및 수출 잠재력이 높은 신시장 개척 지원을 강화하고 있습니다. 최근 동물용 의료기기 업체도 GMP 인증을 받을 수 있도록 했습니다(관련 기사).
이득흔 기자(pigpeople100@gmail.com)