정부가 '대체식품의 표시 가이드라인' 제정(관련 기사)에 이어 '세포배양식품원료'를 '식품원료'로 정식 인정신청할 수 있는 제도 기반을 마련하였습니다. 식품의약품안전처(처장 오유경)는 세포배양 등 신기술을 적용해 생산된 원료를 식품으로 인정받으려는 신청자가 제출해야 하는 자료의 범위를 신설하는 등의 내용을 담은 '식품등의 한시적 기준 및 규격 인정 기준'을 지난 21일 개정‧고시했다고 밝혔습니다(관련 기사). 이번 개정안은 지난해 5월 '식품위생법 시행규칙' 개정으로 세포‧미생물 배양 등 신기술 적용 원료를 식품원료 인정 대상으로 확대됨에 따라, 세포배양식품원료 등의 인정 여부에 대한 제출자료 범위 및 구체적인 절차를 정하기 위해 추진됐습니다. 주요 내용은 ▲세포배양식품원료 등을 한시적 기준‧규격의 인정 대상으로 추가 ▲한시적 기준‧규격을 인정받으려는 신청자가 제출해야 하는 안전성 입증 자료 등 범위 신설(원료명, 세포의 기원, 외래성 오염인자, 제조방법, 단백질·지방·아미노산 등 주요성분, 유해물질 잔류 여부, 알레르기, 유전적 안정성, 독성 등에 대한 자료) ▲인정신청 서식 및 처리기간(270일 이내) 신설 등입니다. 아울러 세포배양식품원료 등 이외의 한

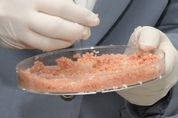
지난 27일 개막한 농림축산식품 과학기술대전에서는 축산물 대체식품과 관련한 기업과 연구소 부스가 적지 않았습니다. 이들은 주로 식물성 원료를 기반으로 한 대체식품 제품을 선보였습니다. 그런데 세포배양물 기술도 홍보되고 있었습니다. 한 기업은 햄버거 패티로 만들어 시식행사도 진행해 참관객의 큰 관심을 모았습니다. 햄버거 패티는 100% 세포배양물이 아닌 식물성 원료와 섞어 만든 것이었습니다. 맛 평가는 차치하고 대체식품의 기술과 전략은 매년마다 빠르게 발전하는 모습입니다. 한편 식품의약품안전처는 최근 마련한 '대체식품의 표시 가이드라인'에서 '배양육' 대신 '세포배양물' 용어를 쓰도록 했습니다(관련 기사). 이득흔 기자(pigpeople100@gmail.com)

식품의약품안전처(처장 오유경, 이하 식약처)는 식물성 원료 등을 사용해 동물성 식품과 유사하게 만든 ‘대체식품’을 제품에 표시하려는 영업자가 준수해야 하는 기준과 방법을 제시하는 '대체식품의 표시 가이드라인'을 마련‧배포하였다고 27일 밝혔습니다. 이번 가이드라인은 대체식품 관련 업계의 다양한 제품 개발을 지원하는 한편 소비자의 알권리와 선택권을 보장하기 위해 마련되었습니다. 대체식품을 제조‧가공‧수입‧소분하는 영업자가 대체식품의 용기 또는 포장에 '대체식품'임을 표시하는 경우에 적용됩니다. 표시해야 하는 항목에는, 대체식품의 주 표시면에 ‘대체식품’임을 명확히 알리는 ▲‘대체식품’ 용어 ▲동물성 식품 등으로 오인‧혼동하지 않도록 하는 제품명 ▲동물성 원료의 포함 여부 등 3가지를 모두 표시해야 합니다. ‘대체식품’이라는 용어는 소비자가 쉽게 확인할 수 있도록 14pt 이상의 글씨로 표시해야 합니다. 제품명은 ‘식물성 제품’임을 강조하거나, 대체한 원재료의 명칭을 포함한 경우에 한해 불고기, 함박스테이크 등 동물성 식품에 사용되는 요리명 등은 사용할 수 있도록 허용했습니다. 다만 오해를 피하기 위해 ‘소고기(쇠고기, 소, 한우, 우육, 비프)’, ‘돼지고기(

9일 청와대 영빈관에서 식품의약품안전처(이하 식약처)가 윤석열 대통령에게 새해 업무보고를 하였습니다. 이날 식약처는 ‘국민 일상을 든든하게, 식의약산업을 단단하게’를 주제로 안전과 규제를 혁신하는 핵심과제를 발표했습니다. 발표 내용에는 푸드테크 산업 지원 방안을 담았습니다. 식약처는 올해 대체식품의 정의, 기준과 표시 가이드라인을 마련하고 세포배양식품의 안전기준을 제시해 이들 식품의 안전한 시장형성을 지원하겠다고 밝혔습니다. 앞서 식약처는 지난달 22일 대체식품 정의·기준 신설 등을 주요 내용으로 하는 '식품의 기준 및 규격' 고시 개정안을 행정예고한 바 있습니다. 이득흔 기자(pigpeople100@gmail.com)