
ASF는 전 세계 양돈산업과 식량안보에 심각한 위협을 가하는 전염성이 강하고 종종 치명적인 질병이다. 수십 년간의 연구에도 불구하고, 안전하고 효과적인 백신은 아직 마련되지 못하고 있는 실정이다. 이전 연구에서, 우리는 야생 분리주를 CA-CAS-01-A 세포에서 연속 계대하여 개발하고 이후 특성을 규명한 새로운 약독화 생백신 후보주인 'ASFV-MEC-01'을 소개했다. 본 연구에서, 우리는 ASFV-MEC-01의 안전성을 추가적으로 평가했다. 구체적으로, 우리는 고병원성 베트남 ASFV 균주에 대한 ASFV-MEC-01의 안전성과 예방 효능을 재확인했다. 주목할 만한 점은 안전성 평가는 임신한 모돈에서도 수행되었다는 것이다. 게다가, ASFV-MEC-01은 대조군 돼지(sentinel pigs; 감시돈)로의 수평 전파 증거를 보이지 않았으며, 연속적인 체내(in vivo) 계대 후에도 병원성으로 회귀하지 않아, 표현형적 안정성을 확인했다. 백신은 또한 접종된 돼지들에서 지속적인 면역 반응을 유도했다. 종합적으로, 이러한 발견들은 ASFV-MEC-01이 유망하고 안전한 약독화 생백신 후보주임을 입증하며, 효과적인 ASF 통제를 위한 가치 있는 도구가 될 수

ASF는 전염성이 매우 높고 치사율이 높아 전 세계 양돈산업과 식량안보에 심각한 위협이 되는 질병이다. 수십 년간의 연구에도 불구하고 안전하고 효과적인 백신은 아직 널리 보급되지 못하고 있다. 본 연구팀은 이전 연구에서 현장 분리주를 CA-CAS-01-A 세포에서 연속 배양하여 개발한 신종 약독화 백신 후보물질 'ASFV-MEC-01'을 소개하고 그 특성을 규명한 바 있다. 본 연구에서는 ASFV-MEC-01의 안전성 지표를 추가로 평가하였다. 특히, 고병원성 베트남 ASF 바이러스 균주에 대한 ASFV-MEC-01의 안전성과 예방 효능을 재확인하였다. 주목할 점은 임신모돈을 대상으로 한 안전성 평가도 수행되었다는 것이다. 또한 ASFV-MEC-01은 '감시돼지(sentinel pigs; 비감염 돼지)'에게 수평 전파되는 증거가 없었으며, 연속적인 생체 내 배양 후에도 독성으로 되돌아가지 않아 '표현형 안정성(phenotypic stability; 약독화 상태 유지)'을 확인했다. 이 백신은 또한 접종된 돼지에서 지속적인 면역 반응을 유도했다. 종합적으로, 이러한 결과들은 ASFV-MEC-01이 유망하고 안전한 약독화 백신 후보물질임을 입증하며, 효과적인 A

ASFV-G-ΔI177L은 상용 백신에 도입된 ASF 바이러스(ASFV) 약독화 생독 균주이다. 본 연구는 임신모돈에서의 안전성과 생체 내 유전적 안정성을 조사하였다. 임신모돈 2마리에 ASFV-G-ΔI177L을 접종한 결과, 한 마리에서 중등도의 ASF 관련 임상증상이 나타났다. 번식성적 측면에서, 자돈의 43%가 사산되었으며 생존한 자돈들은 ASF 특이적 임상증상을 보였고 바이러스혈증이 발생하였다. 연구 종료 시점까지 생존한 비율은 17%에 불과했다. 돼지를 통한 전파 과정에서 ASFV-G-ΔI177L은 3차 및 4차 전파 시 심각한 ASF 특이적 임상증상과 함께 바이러스혈증 증가를 동반하는 등 병원성 회복을 보였다. 전체 유전체 시퀀싱을 통해 C257L 돌연변이가 증식 적합성과 독성 증가의 잠재적 원인으로 확인되었다. 본 연구 결과는 ASFV-G-ΔI177L이 유전적으로 안정적이지 않아 ASF 백신 사용에 안전하지 않음을 보여주며, ASF 백신 후보물질은 임신 동물에서 안전성 시험을 거쳐야 함을 시사한다. [논문 원문(바로보기), African swine fever virus vaccine strain Asfv-G-∆I177l reverts to vir

ASF는 한국의 돼지산업에 중대한 사회경제적 타격을 주는 질병이다. 본 연구는 ASF 발생이 보고된 농장에서 감염된 것으로 보이는 돼지의 ASF 바이러스(ASFV) 혈청양성률을 확인하는 것을 목표로 했다. 이를 위해 한국에서 발생한 ASF 발생 사례(2019–2024년)에서 총 2232개의 혈청을 수집하였다. ASFV 항체 검출을 위해 두 가지 '효소결합면역흡착분석법(ELISA)' 키트를 사용했으며, 세계동물보건기구(WOAH)의 육상동물 진단검사 및 백신 매뉴얼에서 권장하는 방법에 따라 '면역과산화효소검사(IPT)'를 확인 검사로 실시하였다. 또한, 야생멧돼지 개체군 내 ASF 발생 집중 지역을 파악하고, 해당 집중 지역과 ASF 항체 양성 가축 농장 간의 공간적 관계를 평가하기 위해 DBSCAN(Density-Based Spatial Clustering of Applications with Noise) 모델을 이용한 공간 클러스터링을 수행하였다. 그 결과, 항체는 2020년 화천에서 처음 검출되었으나, 2024년까지 ASFV에 대한 검출 가능한 항체를 보유한 돼지는 1.43%에 불과했다. 비록 이 비율은 여전히 낮지만, 항체 양성 돼지의 수는 점차 증가하고

ASF는 사육돼지와 야생멧돼지에서 심각한 질병을 일으키며 대부분 100%의 폐사율을 야기한다. ASF 백신 개발에 최근 가장 많이 연구된 'ASF 바이러스(ASFV)-조지아(ASFV-G)' 균주를 기반으로 한 약독화 균주의 사용은 효과적임이 입증되었다. 2023년 7월, 베트남은 세계 최초로 자체 개발한 ASF 백신 두 종이 현지에서 상업적 판매 승인을 받은 첫 번째 국가가 되었다. 본 연구에서는 ASFV-G-ΔI177L에서 유래한 생백신(LAV) ASFV-G-ΔI177L/ΔLVR의 면역원성과 안전성을 임신한 모돈 5마리와 대조군을 대상으로 분석했다. ASFV-G-ΔI177L은 안정적인 돼지 세포 계통에서 효율적으로 복제된다. 따라서 임신한 모돈을 사용하여 백신의 유효성을 검증했다. 백신 안전성(임상 증상), 분만성적, 출생 후 수직 전파 여부, 모체이행항체 수준은 백신 접종 이후부터 초유 섭취 전후에 걸쳐 평가했다. 백신 접종은 부작용이 없었으며 높은 수준의 항체 생산을 유도했다. 유산 없이 정상적인 분만이 확인되었다. 또한, 백신 접종된 모돈의 초유를 섭취한 대부분의 새끼 돼지에서 ASF 항체와 P72 유전자가 혈액에서 검출되었으며, 백신 접종 후 새끼
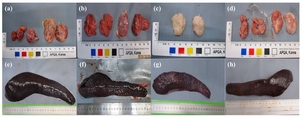
ASF는 돼지에 영향을 미치는 치명적인 전염병이다. 본 연구는 최초의 한국 'ASF 바이러스(ASFV)' 분리주(Korea/Pig/Paju1/2019)를 사용하여 4가지 경로(근육, 구강, 비강, 접촉)를 통해 접종한 돼지에서 각각의 질병 경과를 비교했다. 바이러스 공격 실험에서 근육 접종(IM) 그룹 돼지에게는 '103 HAD50' 1ml을 주사로, '구강 내(IO)' 및 '비강 내(IN)' 그룹 돼지에게는 각각 '106 HAD50' 1ml를 입 또는 콧구멍을 통해 투여하였다. '직접 접촉(DC)' 그룹의 경우 비감염 돼지와 IM 그룹 돼지를 돈방에 함께 수용했다. 연구 결과 IO, IN 및 IM 접종 돼지는 유사한 질병 경과를 보였지만 DC 돼지는 7일 잠복기 후에 비슷한 ASF 증상을 보였다. 가장 흔한 감염 경로 중 하나인 DC 경로의 질병 경과는 IO 및 IN 경로와 유의미한 차이가 없었다. IM 및 DC 그룹은 발열 및 림프절과 비장의 출혈성 병변의 중증도 측면에서 차이를 보였다. 이는 초기 백신 개발 시험에 적합한 IM 경로가 감염 초기 단계를 포함한 ASFV 감염 기전을 연구하는 데 적합하지 않음을 시사한다. 또한, 지정된 용량의 IO 및 IN

ASF는 전염성 바이러스성 질병으로 전 세계 양돈산업에 심각한 위협을 가하고 있다. 한국에서는 2019년부터 ASF 발생이 보고되고 있으며, 순환하는 바이러스(ASFV)의 역학 및 유전적 특성에 대한 포괄적인 이해가 요구되고 있다. 본 연구에서는 '19년부터 '21년까지 국내 양돈장에서 분리된 21개 주의 ASFV를 확보하여 'Illumina MiniSeq'를 사용하여 전체 유전체 염기서열을 분석했다. 최대 가능도 및 시간 척도 접근법을 사용하여 ASFV 분리주의 유전적 관계와 진화적 동향을 분석했다. 21개 주의 ASFV 유전체를 기준 균주인 'Georgia 2007/1'과 비교 분석한 결과, 한국 분리주는 11개의 돌연변이를 공유했지만, 단일염기다형성(SNP)과 삽입/결실다형성(Indel)을 포함한 22개의 개별 돌연변이를 가지고 있는 것으로 나타났다. 계통학적 분석 결과, 모든 한국 분리주는 ASFV 유전자형 II의 아시아 하위 그룹에 속하지만, 최소 세 개의 서로 다른 하위 클러스터로 추가로 구분되는 것으로 나타났다. 시공간적 분석 결과, 북한과의 국경을 넘어 한국으로 ASFV가 여러 차례 유입된 것으로 파악되었다. 또한, ASFV/Korea/Pig/
ASF는 전 세계 양돈산업에 큰 위협이 되고 있다. 이 질병은 한때 특정 지역에만 국한되어 있었다. 하지만 지금은 여러 대륙으로 빠르게 확산되고 있어 연구자들과 양돈농가 모두의 우려가 커지고 있다. 따라서 ASF 바이러스에 대한 백신 개발은 최근 수의학 연구의 최우선 과제가 되고 있다. 생약독화 백신 후보주인 'ASFV-G-ΔI177L/ΔLVR'은 우수한 효능과 안전성을 보였고, 백신 접종 후 ASF 항체가 장기간 지속되었다. 이번 연구는 농장 환경의 변화에 따라 고병원성 동종 ASF 바이러스에 대한 보호 가능성을 평가하고자 했다. 이를 위해 국내 돼지에 ASFV-G-ΔI177L/ΔLVR을 근육 내 접종한 후 병원성이 강한 야외 ASF 바이러스 균주로 공격 접종을 실시했다. 또한 백신을 접종한 돼지에서의 유전체 안정성(genomic stability; 후보주 배출)과 장기 항체 지속성을 평가했다. 평가 결과 백신을 접종한 모든 돼지는 높은 항체 양성률을 보였으며, 공격감염 시점에 더 높은 수준의 항체가 관찰되었다. 이러한 높은 수준의 ASF 백신 항체는 백신 접종 후 약 2개월 동안 유지되었다. 백신을 투여한 지 약 2개월 후에 백신 바이러스 배출이 최소